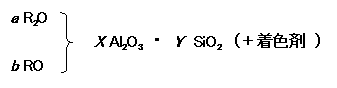
釉薬は「うわぐすり」ともいわれ、陶磁器の素地の上に0.1~0.5mmくらいの厚みで表面をコーティングするガラス状の薄膜です。作品に平滑性、耐汚染性、耐久性、強度、彩飾を与える目的でコーティングされます。日本では古くは桃山時代から織部釉、天目釉、志野釉などが作られ、陶磁器を美しく飾ってきました。
陶芸を趣味としている方は誰もが経験していると思いますが、思った通りの色を出すのは出来合いの釉薬を使ってもなかなか難しいものです。釉薬の調合の方法は無数にあり、それぞれ微妙に異なった色合いを示します。また、釉薬の発色、釉調のメカニズムに関してまだまだ解明されていない部分も多く、概論的に論じるなどというのは暴挙に近いのかもしれません。この章ではそんな釉薬の「科学的な?」一面のほんのさわりの部分を紹介したいと思います。
釉薬を科学的に解説するのにどうしても避けて通れないのがゼーゲル式です。ゼーゲル式はドイツの化学者ゼーゲルによって考案された、釉薬の化学組成を示すもので化学工業としての窯業の世界では頻繁に用いられます(ちなみに陶磁器の焼度を測るゼーゲルコーンも彼の名が由来となっています)。
陶芸家の方で実際ゼーゲル式を使いながら釉薬を調合されている方は少ないでしょうし、実際こんなものを知らなくとも過去の経験則から作られた配合表さえあれば釉薬は調合できます。しかし、釉薬を系統的に理解するには必要な概念ですので、ここではゼーゲル式の基本的な考えとその計算方法を紹介したいと思います。
2‐1‐1. 釉薬の中には何が入っているのか?
まず、釉薬の実際の組成を見てみましょう。ポピュラーなところで織部釉などはどうでしょうか?
表1. 織部釉の調合例
| 原料 | 化学式 | 配合比(%) |
| 長石 | K2O・Al2O3・6SiO2 | 38.7 |
| ドロマイト | MgCO3・CaCO3 | 8.8 |
| 石灰石 | CaCO3 | 7.1 |
| カオリン | Al2O3・2SiO2・2H2O | 12.3 |
| 珪石 | SiO2 | 33.0 |
| 酸化銅 | CuO | 3.0(外割) |
いくつもの原料が織部釉の中に入っていますね。これらの原料は当たり前のことですが、焼成によって作品のアウトラインを飾るにあたりそれぞれ重要な役割を担っています。どこかのスチャラカ社員みたいに遊んでいる原料はひとつもありません。釉薬には一般に以下のような成分が含まれています。
A.骨材(ケイ酸質原料)
ケイ酸(SiO2)は釉薬中で電子受容性(電子を引きつける性質)を持つ酸として振る舞い、釉薬の熔融温度を上昇する働きがあります。ケイ酸を加え過ぎると釉薬が溶ける温度が上昇し、仕上がりが不透明になる傾向があります。逆に少なすぎると粘性が小さくなり、もろくなります。具体的な原料としては珪石、わら灰などがあります。
B.糊材(アルミナ又は粘土質原料)
陶芸の世界でいうアルミナは酸化アルミニウム(Al2O3)、特にα-アルミナを指しますが、代用品として水酸化アルミニウム(Al(OH)3)を用いることもあるようです。アルミナは釉薬中で中性成分として振る舞い、釉薬が溶ける温度には影響しません。アルミナは釉薬が結晶化するのを防ぎ、釉薬の清澄性を促進すると同時に釉薬に適当な粘りを持たせ、厚みを均一にする働きがあります。特に石灰釉には多く使われます。また、アルミナの供給源として釉薬の中にも少量の粘土が入ることがあります。この粘土は、素地と釉薬をスムーズに融着させる役割を持っています。糊材の具体的な原料としてはカオリンやベントナイトが知られています。
| ※アルミナについて 広義におけるアルミナはα-アルミナ(三方晶系のコランダム型構造、空間群:R3c)のほか、超イオン伝導体(導電性の高いイオン結晶。固体電解質とも呼びます)のβ-アルミナ、αの構造多形で欠陥スピネル型構造を有するγ-アルミナ、アルミナ水和物の熱処理で得られるρ、κ、θ、δ、χ、η-アルミナなど、数種が知られています。化学組成の異なるβ(Na2O・11Al2O3)を除いて耐熱性、絶縁性にすぐれるため、絶縁体や熱分析測定用のレファレンス試料として用いられます。また、α-アルミナの単結晶はコランダム(鋼玉)といわれ硬度が大きいのでグラインダーや時計の軸受けに用いられる他、宝石(ルビー,サファイア)に用いられます。 |
C.媒熔剤
釉薬の溶ける温度を調節するために加えられます。釉薬の中では電子供与性(電子を放出しやすい性質)の塩基性成分として振る舞い、多く加えるとそれだけ熔融温度が低下します。カリ(酸化カリウム:K2O)やソーダ(酸化ナトリウム:Na2O)などのアルカリ酸化物や石灰(酸化カルシウム:CaO)などのアルカリ土類酸化物、ホウ酸(B2O3・3H2O)や鉛化合物(酸化鉛:PbOなど)が使われます。具体的な原料としては土灰(木灰)や石灰、酸化鉛や酸化亜鉛が知られています。
D.着色剤
主に釉薬にあざやかな色をつける種々の酸化金属を指します。弁柄(酸化第二鉄:Fe2O3)、酸化第二銅(CuO)、酸化コバルト(CoO)など、一章で述べた遷移元素の酸化物が多く、焼成の雰囲気により微妙にその色調を変化させます。着色剤は配合表に加える場合、外割(残りの原料の総計を100%とし、その百分率で加えること。消費税のようなものです)で記載されることが多いようです。
表1の織部釉の各原料はそれぞれどの役割を担っているのか分類してみましょう。長石とカオリンは糊材と骨材、さらに媒熔剤を兼ねています、ドロマイトと石灰石は媒熔剤、珪石は骨材、酸化銅は着色剤となります。これらの酸性、中性、塩基性成分と着色剤がセットとなって一つの釉薬を形成しています。
2‐1‐2.釉薬の分類指標「ゼーゲル式」
さて、釉薬は骨材、糊材、媒熔剤の3種(場合によっては着色剤も加えた4種)からなっているわけですが、実際はそれぞれの成分が単独の役割を持った原料として存在していることは少なく、例えば長石のように骨材と糊材と媒熔剤の成分が全て入っているものもあるわけです。また一つの成分、例えば媒熔剤の中にも木灰や石灰や酸化鉛など様々な種類のものが存在し、不純物を含むために化学組成が一定しない場合も少なくありません。こうしてみると原料だけで釉薬を系統的に分類するのは困難です。そこで考案されたのがゼーゲル式(Seger
formula)と呼ばれるもので、これは釉薬中の成分を化学式であらわし、それぞれの成分の比を示したものです。一般式の基本形は以下のようになります。
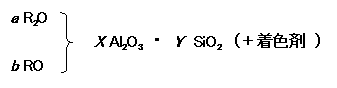
(但し、a+b=1.0)
ゼーゲル式の一番左端のR2OとROは媒熔剤です。ここでR2Oはアルカリ金属の酸化物で酸化リチウム(Li2O)、酸化ナトリウム(Na2O)、酸化カリウム(K2O)または酸化ナトリウムカリウム(KNaO、この物質は実在しないのですが、酸化カリウムと酸化ナトリウムが混在するとき、形式的にこのような表現を用います)です。ROはアルカリ土類金属の酸化物などで酸化マグネシウム(MgO)、酸化カルシウム(CaO)、酸化バリウム(BaO)、酸化鉛(PbO)、酸化亜鉛(ZnO)などです。真中の酸化アルミニウム(アルミナ)Al2O3は糊材です(ごくまれに酸化ホウ素(B2O3)が混じることもあります)。右端のケイ酸SiO2は骨材です(ごくまれに酸化チタン(TiO2)が混じることがあります)。低火度釉などでは少数の例外はありますが、ほとんどの釉薬がこの一般式で表すことができます。それぞれの化学式の係数a,
b, X, Yですが、通常媒熔剤の物質量a+b(この場合重量ではなく、モル数を用います)の合計を1.0とし、糊材Al2O3と骨材SiO2の係数X及びY(モル比)を求めます。
こうして見ると釉薬に使う陶芸原料は着色剤を抜いて100種類以上はゆうにありますが、化学成分としてはせいぜい10数種類どまりであり、ゼーゲル式が釉薬を分類するのに便利であることが分かります。ゼーゲル式は釉薬を分類するのに便利なだけではなく、媒熔剤のバランス、糊材と骨材の比率を読み取ることにより釉調や熔融温度を見積もることができます。
表1の織部釉の化学組成をゼーゲル式で表してみましょう。まず釉薬1000gがあったとすれば、それぞれの原料は、長石387g、ドロマイト88g、石灰石71g、カオリン123g、珪石330g、酸化銅30gとなります。次にそれぞれの成分のモル数を計算します。分子量(化学便覧などから原子量を引っ張ってきて計算します)は長石:556.7、ドロマイト:184.4、石灰石:100.1、カオリン:258.2、珪石:60.1です。原料の重さを分子量で除するとモル数が出ます。それぞれの原料のモル数は表2のようになります。
表2. 織部釉100g中の各原料のモル数(ただし着色剤は含まない)
| 原料 | 化学式 | モル数 |
| 長石 | K2O・Al2O3・6SiO2 | 0.70 |
| ドロマイト | MgCO3・CaCO3 | 0.48 |
| 石灰石 | CaCO3 | 0.71 |
| カオリン | Al2O3・2SiO2・2H2O | 0.48 |
| 珪石 | SiO2 | 5.49 |
これらの原料を骨材、糊材、媒熔剤及び着色剤に分類します。長石は酸化カリウム、酸化アルミニウム及びケイ酸が1:1:6の比で結合したものと組成上みなせるので0.70モルの酸化カリウム及び酸化アルミニウム、そして0.70×6=4.2モルのケイ酸に分解することができます。同様にしてドロマイトは酸化マグネシウム、酸化カルシウムと炭酸ガス、カオリンは酸化アルミニウムとケイ酸と水に分けることができ、表3のように各成分のモル数が決まります。
| 成分 | 原料由来の成分のモル数 | 各成分の合計モル数 |
骨材 |
SiO2(長石由来)0.70×6=4.2 SiO2(カオリン由来)0.48×2=0.96 SiO2(珪石由来)5.49×1=5.49 |
SiO2:4.2+0.96+5.49=10.65モル |
| 糊材 | Al2O3(長石由来)0.70×1=0.70 Al2O3(カオリン由来)0.48×1=0.48 |
Al2O3:0.70+0.48=1.18モル |
| 媒熔剤 | K2O(長石由来)0.70×1=0.70 MgO(ドロマイト由来)0.48×1=0.48 CaO(ドロマイト由来)0.48×1=0.48 CaO(石灰石由来)0.71×1=0.71 |
K2O:0.70モル MgO:0.48モル CaO:0.48+0.71=1.19モル 媒熔剤成分の総計モル数:0.70+0.48+1.19=2.37モル |
それぞれの成分のモル数が決まれば、あとは媒熔剤の総計モル数が1.0になるようにすればよいのですから、各成分のモル数を媒熔剤の総計モル数2.37で除すとゼーゲル式の係数が決まります。したがって表1の織部釉のゼーゲル式は以下のようになります。
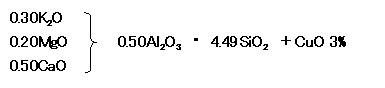
(着色剤は通常外割の重量%で表記します)
上の例では釉薬の原料の組成からゼーゲル式を求めましたが、与えられたゼーゲル式から原料の配分を計算することもよく行われています(というかその方が多いかもしれません)。
なお、ゼーゲル式の導出はExcelなどで計算シートを作成すると便利です(ゼーゲル式計算シートの例)。
ゼーゲル式は同じ成分が複数有る時、本来は上に示すように縦に並べて括弧でくくるのが正しいのですが、今後、このHPでは横に並べて括弧でくくるようにします(いちいち画像ファイルで張りつけていると容量を食ってしまうので・・・)。例えば上の織部釉の組成では
{0.30K2O, 0.20MgO, 0.50CaO}0.50Al2O3・4.49SiO2+CuO 3%
となります(TOP↑)。
釉薬の分類には①焼成温度によるもの、②外観や化学構造によるもの、③着色剤の添加の有無によるもの等様々な切り口があります。ここでは特に②について説明することにします。
2‐2‐1.外観による分類
釉薬の外観(釉調)で分類すると主に5種に分類されます。
・透明釉・・・その名の通り、滑らかで光沢があり、透明な釉調を示す釉薬です。
・失透釉・・・表面は滑らかなのですが、透明釉と違って濁った外観を示します。
・乳濁釉・・・失透釉と同じように見えますが、牛乳のように乳白色の釉調の強い外観を呈します。
・マット釉・・・透明釉や乳濁釉と比べてつや消し調が強くなった釉調を示します。
・結晶釉・・・表面に結晶が成長し文様のようになった釉薬です。
2‐2‐2.化学構造による分類
化学構造で分類すると、釉薬は大きく分けて2種に分類されます。1つは非晶質相のみで形成される釉薬、もう1つは非晶質相に結晶質相が混じる釉薬です。一章で少し触れましたが、分子の配列の仕方によって固体は2つに分類することができます。分子が規則正しく配列しているものを結晶質、不規則なものを非晶質と呼びます。もともと分子は規則正しく配列しようとする性質を持っており、分子量の小さい物質の固体状態はほとんどが結晶質です。しかし、分子量が大きくなると、規則正しく並びにくくなっていきます(図体の大きい人が機敏な動きができないようなものです)。窓ガラスはケイ酸高分子のこうした性質を利用したものです。
2‐2‐1.で述べた5種の分類を化学構造による分類であてはめてみると透明釉及び乳濁釉は非晶質のみで形成され、失透釉、マット釉及び結晶釉は非晶質相に結晶質相が混じる釉薬となります。
1.透明釉
透明釉はゼーゲル式において、糊材と骨材のモル比率Al2O3/SiO2が1/8~1/10の領域で得ることができます。いわゆる透明釉(石灰透明釉、木灰透明釉)やタルク釉などが代表的なものです。
透明釉 :{0.3KNaO, 0.7CaO}0.5Al2O3・4.5SiO2
タルク釉 :{0.5KNaO, 0.5MgO}0.5Al2O3・4.5SiO2
タルク釉は主に磁器に用いられ、白さが際立った釉薬です。
2.失透釉(結晶性乳白釉)
非晶質性のガラス成分の中に微細な結晶性成分が浮遊し、この結晶が光を散乱して乳白しているものです。代表的なものとしてブリストル釉があります。
ブリストル釉 :{0.2KNaO, 0.2CaO, 0.6ZnO}0.5Al2O3・2.5SiO2
ブリストル釉は釉薬中にガーナイト(ZnO・Al2O3)の微細な結晶が生成したものです。ブリストル釉のゼーゲル式を見てみると、透明釉よりもアルミナ成分の割合が大きくなっていることが分かります(Al2O3/SiO2>1/8)。また、アルミナ成分の増大は高温時で融液状となっている釉薬の粘性を高め、結晶は生成するものの大きく成長はせず、細かい結晶が多数析出することになります。
3.乳濁釉(分相性乳白釉)
失透釉と同様乳白した外観を呈しますが、結晶が生成する代わりに非晶質相が2相に分離(分相:phase
separation)してその界面で光の散乱が起こる結果乳白して見えるものです。代表的なものとしてケイ酸分の割合が多い(Al2O3/SiO2<1/10)藁灰釉が挙げられます。
藁灰釉 :{0.2KNaO, 0.2CaO, 0.6ZnO}0.22Al2O3・3.5SiO2
私の経験では単独で上記の釉薬を掛けるより透明釉で下掛けをしておいてその上から乳濁釉をかけた方が藁灰のかすれた乳白がよく出るような気がします。
4.マット釉
失透融と同様、釉中に微細な結晶が多く生成するものですが、内部組織に結晶が析出する失透釉に対してマット釉は表面に結晶が析出するため、全体としてつや消し(マット)調になります。
白マット釉 :{0.3KNaO, 0.7CaO}0.5Al2O3・2.5SiO2
析出する結晶は主にアノーサイト(CaO・Al2O3・SiO2)です。ケイ酸とアルミナの比率は失透釉とほぼ同じであり、失透釉のZnOをCaOに置換したものと言う事ができます。
5.結晶釉
表面に結晶が析出するという点でマット釉と同じですが、ここでいう結晶釉は表面に大きな結晶が成長し、それが文様のようになっているものです。代表的なものとして亜鉛結晶釉があります。ケイ酸とアルミナの比率は透明釉と同じですが、透明釉と比較して媒熔剤の比率が高いのが特徴です。
亜鉛結晶釉 :{0.17KNaO, 0.23CaO, 0.60ZnO}0.17Al2O3・1.60SiO2
析出する結晶はウイレマイト(2ZnO・SiO2)やジオプサイド(2(CaO・MgO)SiO2)です。結晶を大きく成長させるには一旦SK10(1300℃)程度まで上げたのち、1100℃近辺で徐冷することが必要です。これは結晶を成長させるために分子がある程度動きやすい状態にしてやるためです。急冷すると分子が規則正しく配列する前にガラス転移によって釉薬が固化してしまい、結晶が成長しません。有機合成が専門の方は経験があると思いますが、結晶構造解析に用いるような大きな単結晶を作る場合、再結晶の際に徐冷することが多いのと同じです。
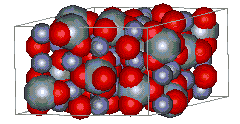
図2‐1.ウィレマイトの結晶構造(赤:酸素 銀:ケイ素 水色:亜鉛)
2-2-3.化学組成と釉調との関係
2-2-2.で述べた5種の釉薬の化学組成と性状を大まかにまとめたものが図1の状態図です。縦軸がアルミナ、横軸がケイ酸のモル数を表しています。但し、それぞれの領域の組成であれば必ずその釉調になるというわけではなく、焼成時の温度管理、焼成時間によってもかなり左右されます(TOP↑)。
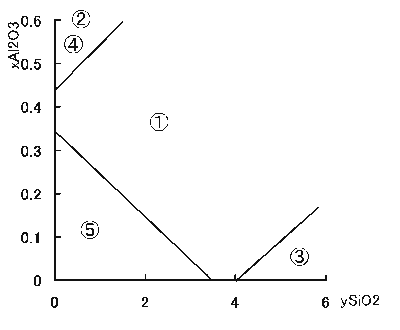
図2‐2.化学組成と釉調を示す状態図。①透明釉 ②失透釉 ③乳濁釉 ④マット釉 ⑤結晶釉
2-3.興味深い釉調のメカニズム
2‐2.述べたように釉薬はその化学組成により独特の外観を示します。科学的にその原因が解明されているものはごく少ないのですが、ここではそのいくつかを紹介してみたいと思います。
2‐3‐1.分相の科学
白萩釉などに代表される乳濁釉は乳白した外観を示すのが特徴です。先に述べたようにこれは非晶質相が2相に分離することに起因しています。電子顕微鏡で乳濁釉の組織をみると図2‐2のように球形の粒子が液体の中に浮かんでいるような像が観察されます。液体のように見える部分(マトリクス相:matrix
phase)と粒子の部分(分離相:separation phase)の界面で光による散乱が起きる結果、乳白した外観を示すのです。分相はあるときは外観における「味」となり、あるときには耐久性を損なう原因になったりします。

図2‐3. 乳濁釉を電子顕微鏡で見たときの模式図、
灰色部分がマトリクス相、青の部分が分離相
参考文献の「陶磁器釉の科学」によると分相を起こしやすい釉組成としては藁灰釉の他に下記のようなものが挙げられています。
亜鉛乳白釉 :{0.2KNaO, 0.2CaO, 0.6ZnO}0.22Al2O3・3.5SiO2
鉛ホウケイ酸フリット :{1.3PbO}1.8B2O3・4.7SiO2
鉛ホウケイ酸フリットはホウ酸塩ガラス相とケイ酸塩ガラス相とに分離しています。
分相は時として陶磁器にとって好ましくない方向に働くこともあります。そこで、分相を防ぐためには糊材であるアルミナを多く添加してやると有効な場合が多いようです。アルミナ分が増えれば2‐2‐2.でのべた透明釉の組成に近づきます。
| ※分相の学術的研究 分相はガラス性材料においてはごくありふれた現象で、材料工学、無機化学分野では様々な研究が進んでいます。分相の起こる原因は熱力学的には2成分系の高温領域における組成-Helmholtzの自由エネルギー(F)曲線が1つの極小を持つのに対し、それを冷却していくとエネルギー鞍点を生じて2つのエネルギー極小を持つことで説明されています。しかし、熱力学的に説明がついてもそれをガラスの化学構造とリンクさせて具体的なイメージとしてとらえるのは容易なことではありません。そこで統計力学の概念を導入してこれらを説明しようという試みが行われています。 {0.2(1‐x)Na2O, }0.2(1‐x)B2O3・xNaCl(xは0以上1以下の数) とし、原子間に働く力(力場といいます)をNewton方程式で規定してから原子の動きをシュミレーションします。 上記の組成のガラスは酸素原子を介してホウ素原子がつながっているネットワーク構造を形成していることが知られています。酸素原子は通常2つのホウ素原子と結合してネットワーク構造の「つなぎ」役となっているのですが、その中には、結合しているホウ素が1つしかない「非架橋酸素」と呼ばれる変わり者がいて、ネットワーク構造をところどころで寸断しています。 ・コンピュータの処理能力に限界があり、釉薬のように化学組成の複雑な系は取扱うことができない。 ・力場が経験的なもので汎用性に乏しいため、現象の予測という点では精度を欠く 現在のコンピュータハードの進歩は目覚しく、力場についても量子力学を導入した非経験的で理論的に厳密なものが考案されています(当然計算時間はその分長くなるのですが)。 |
2-3-2.貫入の生成機構
To Be Continued....